ミロガバリン(タリージェ)の第三相臨床試験をまとめ読みした件
<はじめに>
先日職場でタリージェ(ミロガバリン)の勉強会があったので、承認審査資料(審査報告書)と根拠となった二つの第三相臨床試験を事前に読んでみました。
採用の見込みはほぼなさそうな気配なので、せめて勉強した内容を簡単に吐き出したいのでここに書いてみることにしました。
<今回の資料>
タリージェ審査報告書(pdf注意)
http://www.pmda.go.jp/drugs/2019/P20190122001/430574000_23100AMX00014_A100_1.pdf
糖尿病性末梢神経因性疼痛のPhaseⅢ(J303試験)
https://www.ncbi.nlm.nih.gov/pubmed/?term=30672128
PMID: 30672128
糖尿病性末梢神経因性疼痛のPhaseⅢの事前登録
https://clinicaltrials.gov/ct2/show/record/NCT02318706
帯状疱疹後神経痛のPhaseⅢ(J304試験)
https://www.ncbi.nlm.nih.gov/pubmed/?term=30913164
PMID: 30913164
帯状疱疹後神経痛のPhaseⅢの事前登録
https://clinicaltrials.gov/ct2/show/record/NCT02318719
<糖尿病性末梢神経因性疼痛の方を読んでみる>
P:20歳以上の糖尿病(1型2型どちらでもよい)で糖尿病性末梢神経因性疼痛のあるアジア人834名。→ADPS(平均1日疼痛スコア)4~9点、VAS40~90mm、HbA1C10%以下(NGSP値)、Ccr60mL/min以上、アジアの詳細=日本、韓国、台湾、マレーシア
※ADPS=過去24時間にわたる疼痛を数値評価尺度(0 =「無痛」〜10 =「最悪の痛み」)で評価
I/C:ミロガバリン1日15mg、20mg、30mg、プラセボ(1:1:1:2)
O:(主要評価項目)14週でのADPSの変化量
(副次評価項目)反応率(ADPS改善率30%、50%の患者の割合)、VAS、ADSIS(1日平均睡眠干渉スコア)、PGIC(患者の全体的変化の印象)、有害事象
※ADSIS=過去24時間の0 = "痛みは睡眠を妨げなかった"から10 = "痛みは完全に睡眠を妨げた"の数値スケールで毎朝評価し週で平均にしてスコア化
※PGIC=患者は治療の終わりに0 =「非常に改善」から7 =「非常に悪い」までのスケールで評価
※ADPS改善率30%のみ結果でいきなり出てくる事前に示されていない評価項目。
なお、副次評価項目はすべて事前登録情報には記載がない。
ランダム化:層別ランダム化(ADPS6点未満、6点以上)
隠蔽化: 「Interactive Web Response System」とあり割り付けは隠蔽化されていると思われる
施行バイアス:プレガバリン、抗てんかん薬、セロトニンおよびノルエピネフリン再取り込み阻害薬、催眠薬(ゾルピデムなどの超短時間作用を除く)および抗不安薬、ならびにオピオイドが禁止。アセトアミノフェンの頓服は許可。
ITT:mITT(脱落欠損値はLOCFで補完)
サンプルサイズ:論文中に記載はないが、審査資料・事前登録情報によると750名のよう(検出力90%、α=0.05、ADPSの差0.6で計算)
追跡率:824(解析に回った人数)÷834(ランダム化された人数)=98.8%
結果:
Table1(ベースライン):平均61.4歳、男性72.5%、体重69.08kg、Ccr99.8、ADPS5.59、2型糖尿病96.3%、神経障害の期間43.0か月、HbA1C7.50%、日本人72.3%
ADPS(主、対プラセボ):15mg -0.03(-0.35~0.30)、20mg -0.15(-0.48~0.17)、30mg -0.50(-0.82~-0.17)
反応率(30%):プラセボ 36.5%、15mg 39.0%、20mg 36.0%、30mg 44.5%
反応率(50%):プラセボ 19.0%、15mg 21.0%、20mg 20.0%、30mg 31.0%
VAS:プラセボ -16.6、15mg -16.8、20mg -18.1、30mg -22.5
ADSIS:プラセボ -0.91、15mg -1.06、20mg -1.04、30mg -1.47
PGIC:やや改善(プラセボ 58.8%、30mg 70.3%)、よく改善(プラセボ 26.1%、30mg 40.0%)
有害事象:プラセボ 61.2%、15mg 68.3%、20mg 68.5%、30mg 77.6%
(有害事象は論文で示されていなかったので、審査資料より)
鼻咽頭炎:プラセボ 12.7%、15mg 13.4%、20mg 14.5%、30mg 16.4%
眠気:プラセボ 3.9%、15mg 8.5%、20mg 12.1%、30mg 14.5%
めまい(中止の最大の原因):プラセボ 2.1%、15mg 4.9%、20mg 8.5%、30mg 10.9%
浮腫:プラセボ 1.2%、15mg 4.9%、20mg 2.4%、30mg 8.5%
体重増加:プラセボ 0.6%、15mg 2.4%、20mg 3.0%、30mg 6.7%
外傷:プラセボ 1.8%、15mg 1.2%、20mg 1.8%、30mg 5.5%
※鼻咽頭炎と外傷は審査資料にはない
まとめ:30mgのみプラセボに対して有意差を示した。有害事象は類薬のリリカ(プレガバリン)に似た感じ。
<帯状疱疹後神経痛の方を読んでみる>
P:20歳以上のアジア人帯状疱疹後神経痛患者765名
→VAS40~90mm、ADPS4~9、Ccr60mL/min以上
I/C:ミロガバリン1日15mg、20mg、30mg、プラセボ(1:1:1:2)
O:(主要評価項目)14週でのADPSの変化量
(副次評価項目)反応率(ADPS改善率30%、50%の患者の割合)、VAS、ADSIS(1日平均睡眠干渉スコア)、PGIC(患者の全体的変化の印象)、SF-MPQ、HADS、SF-36、アロディニアの有無、痛覚過敏の有無、有害事象
※副次評価項目はすべて事前登録情報には記載がない。
ランダム化:層別ランダム化(ADPS6点未満、6点以上)
隠蔽化: 「Interactive Web Response System」とあり割り付けは隠蔽化されていると思われる
施行バイアス:プレガバリン、抗てんかん薬、催眠薬および抗不安薬、オピオイド、トラマドール(合剤含む)、ノイロトロピン、NMDA受容体拮抗薬、筋弛緩薬、ビタミンB1、B12などが禁止。抗うつ薬、睡眠薬、NSAIDs、漢方は試験前からの服用に限り同用量なら許可。
ITT:mITT(脱落欠損値はLOCFで補完)
サンプルサイズ:論文中に記載はないが、審査資料・事前登録情報によると750名のよう(検出力90%、α=0.05、ADPSの差0.6で計算)
追跡率:763(解析に回った人数)÷765(ランダム化された人数)=99.7%
結果:
Table1(ベースライン):66.5歳(75歳以上は平均18.3%だが20mg群が27.5%と突出している印象)、男性60.3%、体重62.3kg、ADPS5.71、VAS59.1、罹病期間18.0か月
変化量(MD)(対プラセボ)
ADPS:15mg -0.41(-0.74~0.07)、20mg -0.47(-0.81~0.14)、30mg -0.77(-1.10~-0.44)
VAS:15mg -5.1(-0.88~-1.4)、20mg -5.7(-9.4~-1.9)、30mg -7.8(-11.5~-4.1)
ADSIS:15mg -0.50(-0.81~-0.19)、20mg -0.48(-0.79~-0.17)、30mg -0.76(-1.07~-0.45)
変化率(OR)(対プラセボ)
反応率(30%):15mg 1.54(1.03~2.29)、20mg 1.52(1.02~2.27)、30mg 1.81(1.21~2.69)
反応率(50%):15mg 1.20(0.75~1.93)、20mg 1.48(0.93~2.34)、30mg 1.63(1.04~2.56)
PGIC(2点以下):15mg 1.58(1.04~2.40)、20mg 1.39(0.91~2.13)、30mg 1.45(0.95~2.20)
PGIC(3点以下):15mg 1.39(0.94~2.08)、20mg 1.89(1.25~2.85)、30mg 1.86(1.24~2.81)
有害事象(治療関連で5%以上のもの)
鼻咽頭炎:プラセボ 8.6%、15mg 8.6%、20mg 10.5%、30mg 12.9%
眠気:プラセボ 3.6%、15mg 13.2%、20mg 17.0%、30mg 23.9%
めまい:プラセボ 2.1%、15mg 4.9%、20mg 8.5%、30mg 10.9%
浮腫:プラセボ 0.7%、15mg 1.3%、20mg 3.9%、30mg 7.1%
体重増加:プラセボ 0.3%、15mg 4.6%、20mg 5.2%、30mg 5.2%
<まとめ>
メーカーは受容体への選択性の高さから「既存薬より安全である可能性」を売り文句にしていた。あと「直接比較したデータはない」と言っていたのが気になった。
で、既存薬であるリリカと直接対決した貴重なPhaseⅡ試験の結果を見てみる(審査資料より)
P:糖尿病性末梢神経因性疼痛患者
I/C:プラセボ、プレガバリン300mg/日、ミロガバリン1日10mg、20mg、30mg
O:7週でのADPSの変化量
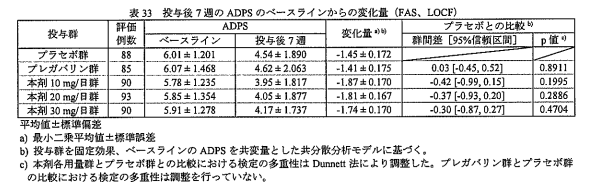
全介入群でプラセボに対し有意差を認めなかった。
で、肝心の安全性は
有害事象:プラセボ 53.4%、プレガバリン 58.1%、10mg 48.9%、20mg 63.4%、30mg 73.3%
治療関連有害事象:プラセボ 15.9%、プレガバリン 36.0%、10mg 17.8%、20mg 30.1%、30mg 47.8%
特にミロガバリンで有害事象が少ないというわけではないよう。
全体を通して積極的に使う理由も見当たらない感じなので、「当面様子見」というのが整形外科医のいない職場での結論になりそうです。